鄭州源創基因科技有限公司成立于2016年,由哥倫比亞大學博士后趙輝,歸國創辦的國家高新技術企業。擁有97項知識產權及實用技術,業務遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區。
2025年7月29日,國際頂尖期刊《Signal Transduction and Targeted Therapy》(STTT)在線發表了一項開創性研究,為深陷治療困境的失代償性肝硬化(DLC)患者帶來了新的曙光。

這項由中國人民解放軍總醫院第五醫學中心、國家感染性疾病臨床研究中心王福生院士領銜的團隊完成的I期臨床試驗,首次系統性地在人體內探索了間充質干細胞(MSC)治療DLC的安全劑量、關鍵作用機制,為尋找肝移植之外的有效療法邁出了關鍵一步。
失代償性肝硬化的困境與干細胞潛力
失代償性肝硬化(DLC)是肝硬化進展的嚴重階段。此時,患者不僅面臨嚴重的肝功能衰竭,還伴隨著復雜的免疫失調——表現為一種矛盾狀態:全身炎癥反應過度活躍的同時,機體抵抗感染的能力卻顯著下降,導致患者極易發生感染,病情迅速惡化。
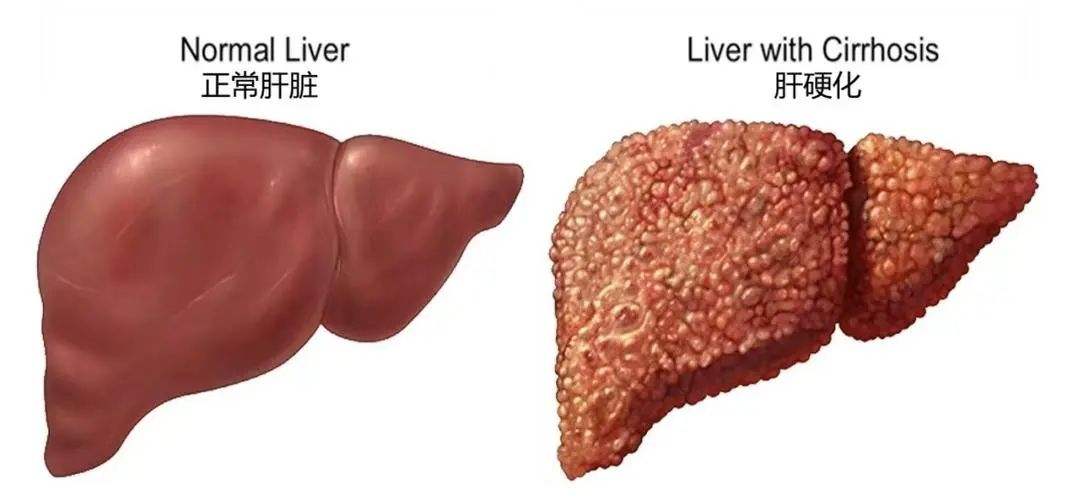
目前,肝移植是唯一能根治DLC的方法。然而,供體肝臟嚴重短缺、手術風險高以及費用昂貴,使得絕大多數患者難以獲得移植機會。據國內研究數據估算,我國現有肝硬化患者約700萬-800萬人,其中處于失代償期的患者數量達百萬級別,治療需求巨大。
間充質干細胞(MSC)因其強大的免疫調節和組織修復潛能,被視為治療DLC的潛在希望。既往研究表明,MSC可能通過平衡免疫反應、促進損傷修復來改善肝硬化癥狀。然而,MSC治療DLC的最佳劑量、給藥方式以及在人體內的確切作用機制尚不清楚,這嚴重阻礙了其臨床應用。為了填補這一空白,王福生院士團隊精心設計了這項劑量遞增的I期臨床試驗。
研究設計:系統探索安全劑量
研究分為兩個階段,共納入24名中位年齡51歲的中重度DLC患者(Child-Pugh評分中位數8.12分),病因主要為乙肝病毒和酒精。
Ia期(單劑量試驗):采用“3+3”劑量遞增設計。4組患者分別單次輸注不同劑量MSC(5.0×10?至2.0×10?細胞)。治療后密切隨訪28天,并運用單細胞RNA測序等先進技術分析免疫細胞動態變化。
Ib期(多劑量試驗):基于Ia期結果,選取兩個劑量組(1.0×10?和2.0×10?細胞/次),患者每周接受1次輸注,共3次,隨訪至28天,評估多劑量方案的安全可行性。
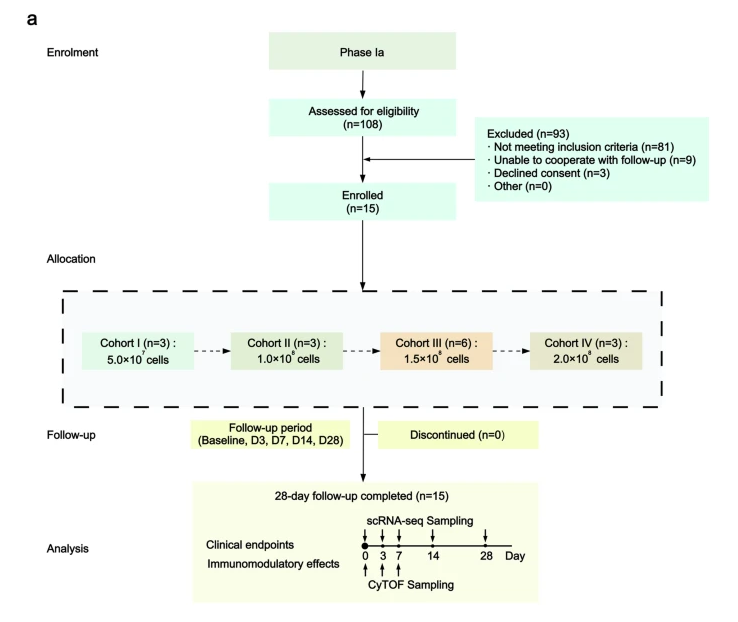
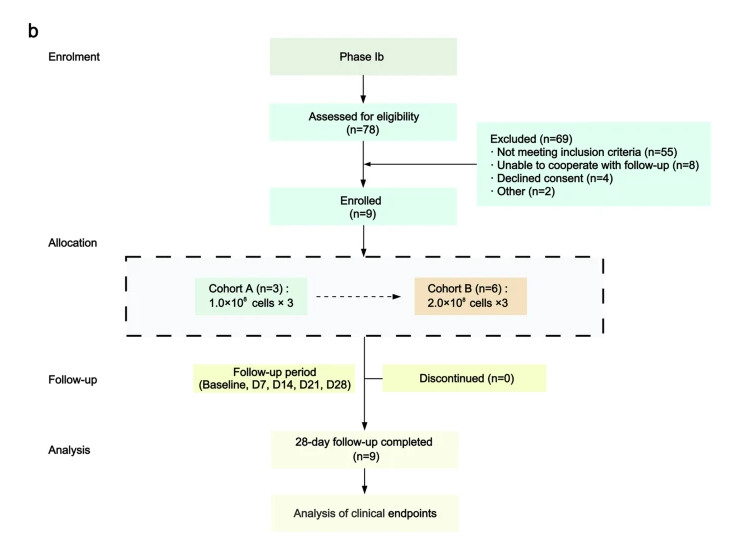
關鍵發現:安全可控、機制明朗、療效初顯
經過28天的嚴密監測,該研究取得了多項突破性進展:
安全可靠:所有患者(包括單次高劑量和多次給藥)均未發生嚴重不良事件或劑量限制性毒性。僅報告少數輕微反應(如短暫皮疹、低熱),程度輕且與MSC輸注相關性低。這為后續研究提供了堅實的安全基礎。
機制明朗:研究發現MSC的免疫調節效果具有劑量依賴性——高劑量組(尤其是2.0×10?細胞)效果更顯著。研究首次在人體內鎖定關鍵作用靶點:MX1+ 單核細胞。
這類細胞在DLC患者體內異常增多且高度活躍(促炎)。
MSC輸注后,尤其在高劑量下,能顯著減少MX1+單核細胞數量并抑制其功能活性。
這種有益變化在治療后第7天達峰,14天后減弱,提示未來需優化給藥間隔以維持效果。
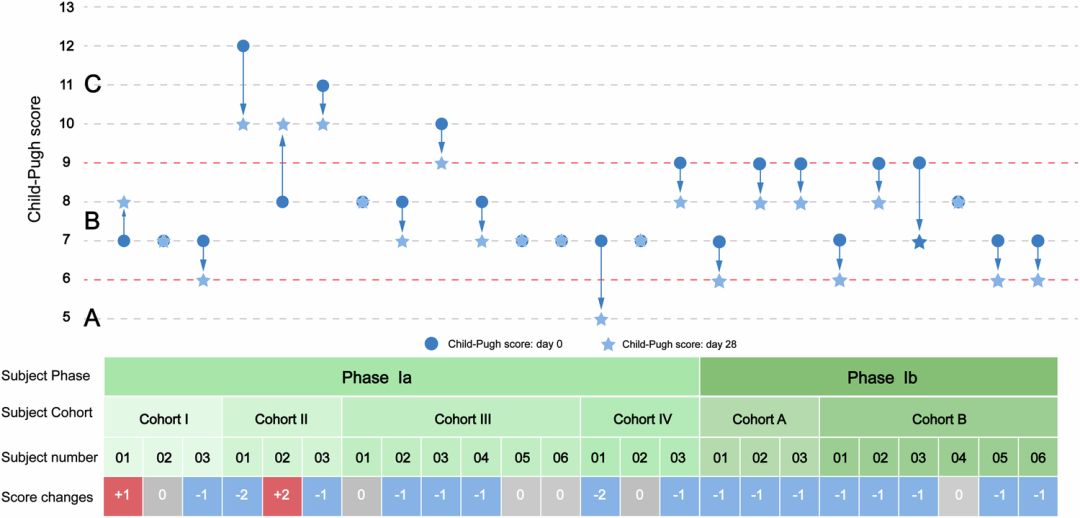
療效初顯:盡管主要評估安全性,但也觀察到積極的臨床改善信號,且在高劑量與多劑量組更明顯:
肝功能:白蛋白、膽堿酯酶等合成功能指標有提升趨勢;Child-Pugh和MELD等關鍵評分觀察到下降趨勢。
生活質量:多劑量組患者的慢性肝病問卷(CLDQ)評分顯示改善趨勢(報告改善率88.9%),提示癥狀(如疲勞、腹脹)可能緩解。
意義與展望
這項開創性的I期臨床試驗意義重大,首先證實了MSC治療失代償性肝硬化在選定劑量方案下的安全性;且首次在人體內系統闡明了MSC的劑量效應關系,并揭示了其通過抑制過度活躍的MX1+單核細胞來調節免疫的關鍵作用機制,識別了潛在的療效生物標志物。

這些發現如同繪制了一張精準的“治療導航圖”,為未來優化MSC治療方案(如最佳劑量、頻次)和實現個體化精準治療奠定了科學基石。雖然仍需更大規模試驗驗證長期療效和確定最終方案,但對于數百萬DLC患者而言,這項研究無疑點亮了一盞充滿希望的明燈。
間充質干細胞療法正加速從實驗室的“潛在可能”邁向臨床應用的“現實希望”。未來,它有望成為肝移植的有力補充,為終末期肝病患者提供一條更可及、更安全的生命新通道。
https://mp.weixin.qq.com/s/6k5y5wMRcsLeGxWuqnGblw
https://www.nature.com/articles/s41392-025-02318-4