鄭州源創基因科技有限公司成立于2016年,由哥倫比亞大學博士后趙輝,歸國創辦的國家高新技術企業。擁有97項知識產權及實用技術,業務遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區。
缺氧性肺動脈高壓(Hypoxic Pulmonary Hypertension, HPH)是一種由長期低氧環境(如慢性阻塞性肺疾病、慢性高原病等)引發的進行性肺血管疾病,其特征為肺動脈壓力持續升高,最終可能會因右心衰竭而導致死亡。
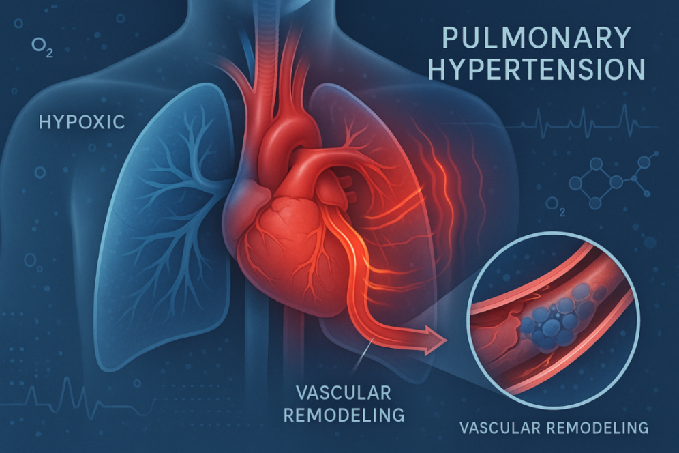
該病病理進程涉及肺血管重構,包括肺動脈平滑肌細胞異常增殖、血管壁增厚及纖維化,顯著增加右心室后負荷,盡管現有擴血管藥物可緩解癥狀,但對疾病進程的逆轉作用有限,部分重癥患者僅能通過肺移植維持生命。
干細胞外泌體:靶向調控病理機制的新策略
南京醫科大學附屬蘇州醫院與蘇州大學聯合團隊在《Scientific Reports》(2025年7月)發表研究,首次系統揭示了骨髓間充質干細胞外泌體(MSC-exo)通過精準調控關鍵信號通路,有效逆轉HPH病理進程的分子機制。

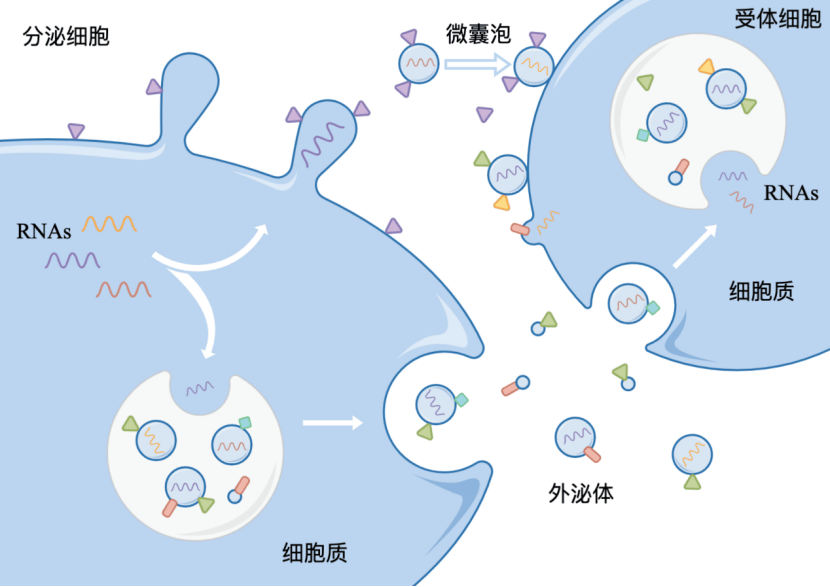
干細胞外泌體:細胞間通信的“納米信使”
外泌體是細胞分泌的納米級細胞外囊泡(直徑30-150 nm),內含蛋白質、脂質、mRNA及非編碼RNA等多種生物活性分子,可通過旁分泌或內分泌方式精準調控靶細胞功能。相較于干細胞移植,外泌體具有低免疫原性、無致瘤風險、易于保存等優勢,被視為“無細胞治療”的典型代表,為細胞領域開辟了2.0時代新方向。
核心發現:阻斷EGFR/ErbB2異二聚體信號通路
研究通過體外細胞實驗與體內動物模型(HPH大鼠)證實,HPH的關鍵病理驅動因素是肺動脈平滑肌細胞(PASMC)異常增殖與遷移,而這一過程高度依賴表皮生長因子受體(EGFR)與ErbB2受體形成的異源二聚體(EGFR/ErbB2)信號通路激活。MSC-exo可通過遞送特定miRNA(如miR-145、miR-126等),直接抑制EGFR與ErbB2的磷酸化及下游PI3K/AKT、MAPK信號傳導,從源頭阻斷血管重構的分子開關。
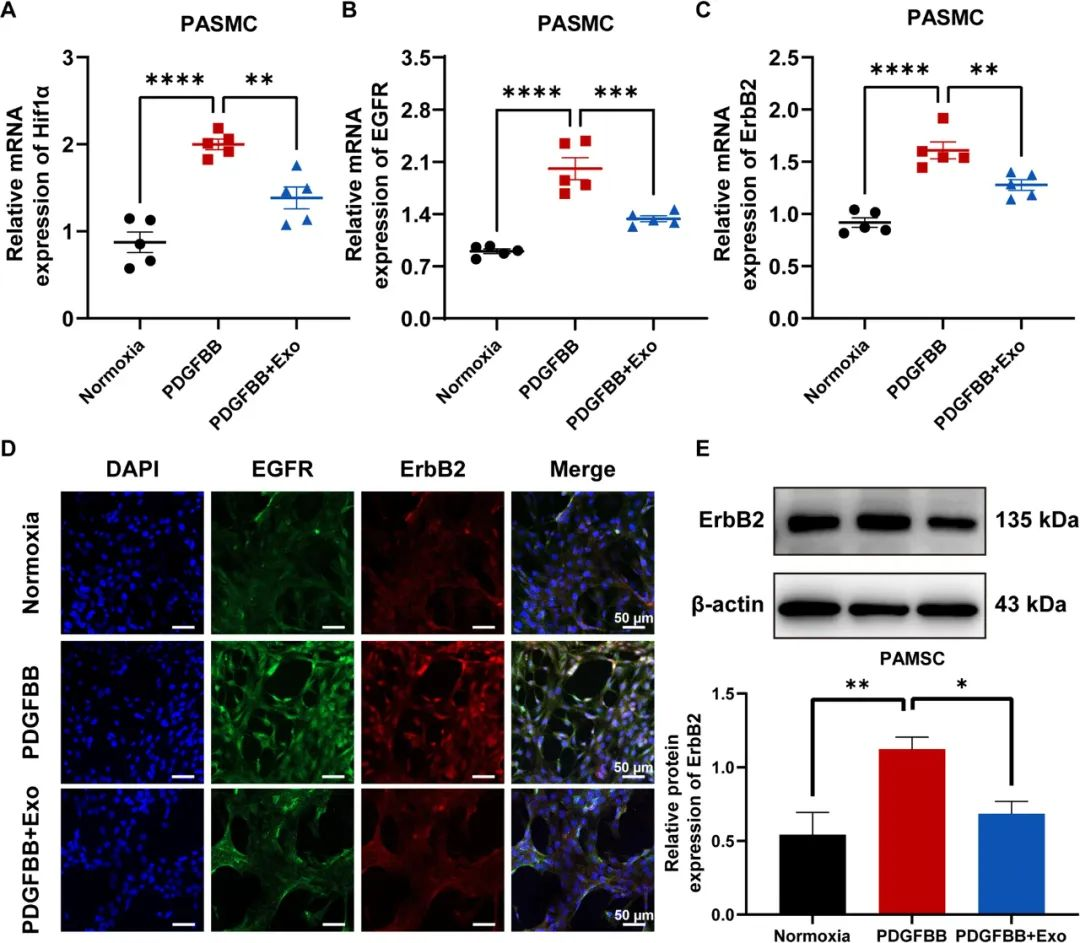
動物實驗驗證:多維度病理指標改善
在HPH大鼠模型中,靜脈注射MSC-exo(每周2次,持續4周)后觀察到:
血流動力學改善:平均肺動脈壓(mPAP)降低32.7%,右心室收縮壓(RVSP)下降28.4%;
結構逆轉:肺小動脈中膜厚度占比(MT%)減少41.2%,血管周圍纖維化面積降低38.6%;
分子標志物調控:肺組織中HIF-1α(低氧誘導因子-1α)、EGFR、ErbB2及下游p-AKT蛋白表達顯著下調(p<0.05)。
研究結果表明,MSC-exo不僅可改善HPH的臨床癥狀,更能從分子水平實現“精準打擊”,為疾病治療提供明確靶點。
小結
該項研究首次明確了MSC-exo通過抑制EGFR/ErbB2異二聚體信號治療HPH的分子機制,為外泌體療法在難治性心肺疾病中的應用奠定了實驗基礎。未來可基于該靶點開發特異性外泌體制劑或小分子抑制劑,有望突破傳統治療的局限性。
需注意的是,當前成果仍局限于動物模型階段,后續需通過多中心臨床試驗驗證其安全性與有效性。但毫無疑問,干細胞外泌體作為“天然藥物載體”,正成為肺動脈高壓精準醫療領域最具潛力的研究方向之一。
https://mp.weixin.qq.com/s/a241r8hfWjRK0ntK7rm3lw?click_id=49
Chen, YX., Deng, ZH., She, XW. et al. Mesenchymal stem cell-derived exosomes improve vascular remodeling by inhibiting EGFR/ErbB2 heterodimerization in hypoxic pulmonary hypertension. Sci Rep 15, 24303 (2025).